1.
Канонический набор аминокислот
1.1. Что
такое аминокислоты
Живые существа
состоят из различных типов структур, в том числе белков. Аминокислоты входят в
состав белков в виде остатков, отдельных звеньев. Звенья аминокислот в белках
можно выделять по-разному. На нашей
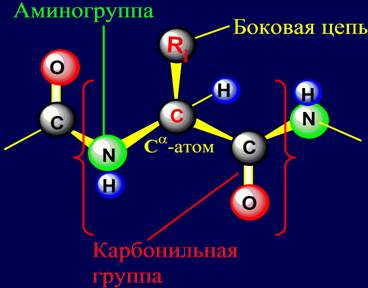
страничке звено выделяется так (рис.1):
|
Рис. 1. Звено аминокислоты в цепи белка |
|
1.
Звено находится в фигурных скобках, обозначенных красным цветом
2.
В центре звена – Ca-углеродный атом, связи которого имеют форму тетраэдра.
3.
Слева находится аминогруппа звена (зеленого цвета), справа –
карбонильная группа (содержит атом кислорода красного цвета);
4.
Сверху к Ca-углеродному атому присоединена боковая цепь аминокислоты
(обозначена буквами Ri). Буква i
может принимать
разные числовые значения. Если
боковые цепи пронумеровать от 1 до 20, то буква i будет принимать значения
от 1 до 20.
5.
К тетраэдрическому Ca-углеродному атому присоединен также
атом водорода (синего цвета).
1.2.
Как выглядят боковые цепи аминокислот
Существуют различные классификации боковых цепей аминокислот. Мы
представим классификацию боковых цепей, которая довольно часто встречается в
учебных пособиях. Эта систематизация подразделяет боковые цепи аминокислот на
три группы:
1. Неполярные
2. Слабо полярные и
полярные
3. Циклические
|
Неполярные боковые цепи |
|||||
|
Неполярные боковые цепи не содержат полярных групп и не образуют водородных связей |
|||||
|
К
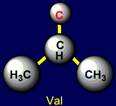
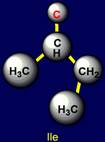
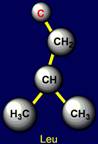
этой группе относят: глицин (Glycine - Gly), аланин (Alanine - Ala), валин (Valine – Val), изолейцин (Isoleucine – Ile), лейцин (Leucine – Leu). Глицин
не имеет боковой цепи. Самая
короткая боковая цепь – у аланина, самая
длинная - у лейцина. |
|
|
|
|
|
|
Глицин |
Аланин |
Валин |
Изолейцин |
Лейцин |
|
|
Слабо полярные и полярные боковые цепи |
|||||
|
Как правило, боковые цепи этой группы образуют водородные
связи. Эти связи образуются между двумя атомами через атом водорода и
записываются так: XH…Y. Водородные связи бывают протонодонорные, когда атом водорода
присоединен к атому Х, и протоноакцепторные, когда атом,
образующий водородную связь (Y), не имеет атома водорода.
Протонодонорные водородные связи образуют группы: ОН серина и треонина, О=С-ОН – аспарагиновой
и глютаминовой кислот, О=С-NH2 –аспарагина и глютамина, С-NH2 – лизина, HN=C-NH2 – аргинина, SH - цистеина. Протоноакцепторные водородные связи образуются с
атомами О аминокислот серина,
треонина, аспарагиновой и глютаминовой кислот, аспрагина и глютамина, а также с атомом S
метионина. |
|||||
|
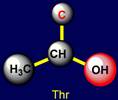
К слабо полярным
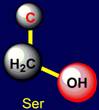
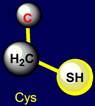
относятся: cерин (Serine – Ser) и треонин (Threonine – Thr), которые содержат C–ОН группу, а также цистеин
(Cysteine – Cys), имеющий группу C–SH. Полярными являются боковые
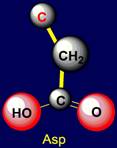
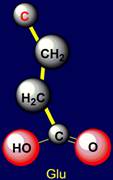
цепи: аспарагиновой (Aspartic acid – Asp) и глютаминовой кислот (Glutamic acid – Glu), содержащие O=C–OH группу,
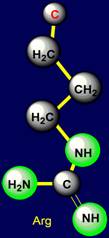
а также аргинин
(Arginine – Arg), с гуанидиновой
группировкой (группа N=C–NH) и лизин
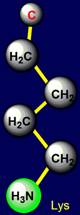
(Lysine – Lys) с аминогруппой (C–NН2). Нейтральными,
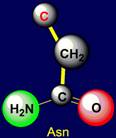
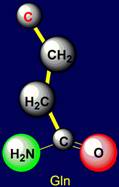
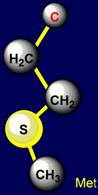
образующими Н-связи являются: аспарагин (Asparagine – Asn), глютамин (Glutamine – Gln), имеющие
группу O=C–NН2 и метионин (Methionine – Met), содержащий атом серы (группа C–S) |
|
|
|
|
|
|
Серин |
Аспарагиновая кислота |
Глютаминовая кислота |
Аргинин |
Лизин |
|
|
|
|
|
|
|
|
|
Цистеин |
Треонин |
Аспарагин |
Глютамин |
Метионин |
|
|
Циклические боковые цепи |
|||||
|
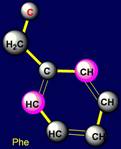
Все циклические аминокислоты, кроме пролина, образуют водородные связи. Фенилаланин образует слабые водородные связи за счет СН-групп, которые выделены в молекуле розовым цветом |
|||||
|
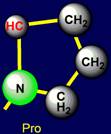
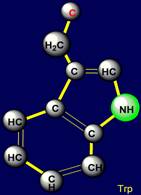
Циклические боковые цепи: пролин (Proline – Pro) , его 5-членный цикл
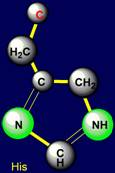
входит в основную цепь белка; гистидин (Histidine –
His), триптофан (Tryptophane – Trp), все они имеют
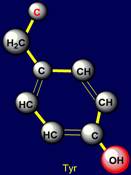
5-членные циклы, фенилаланин Phenylalanine – Phe), тирозин
(Tyrosine – Tyr), содержат 6-членные циклы |
|
|
|
|
|
|
Пролин |
Гистидин |
Триптофан |
Фенилаланин |
Тирозин |
|
Знание структуры боковых цепей аминокислот поможет Вам в
понимании принципов построения модели пространственной
структуры канонического набора аминокислот. При необходимости вспомнить
ту или иную аминокислоту, можно заглянуть в этот раздел.
Следующим этапом нашей работы было построение на додекаэдре
модели структуры из двадцати формальных элементов. Модель описана в разделе 2.
Адрес для связи: amino-acids-20@yandex.ru