4.2.1. Квази-зеркальная антисимметрия
|
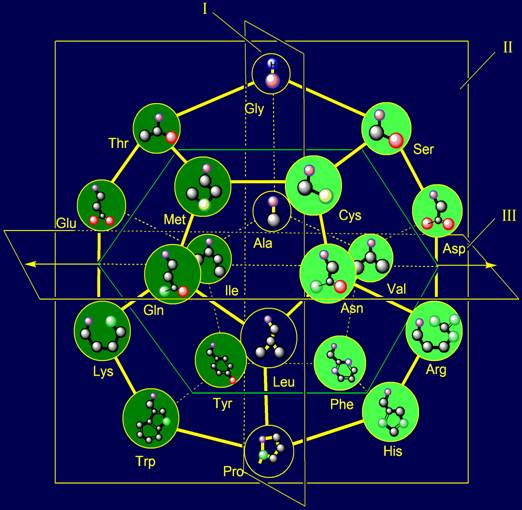
Антисимметричные аминокислоты, располагающиеся по обе стороны
от плоскости I,
которую мы назвали плоскостью квази-зеркальной
антисимметрии образуют пары, обладающие близкими
физическими свойствами, но разной длиной цепи или массой. Справа от плоскости
I оказались
более короткие или более легкие боковые цепи (они показаны на светло-зеленом
фоне), а слева – более длинные или тяжелые (темно-зеленый фон). Чтобы это
видеть более детально, боковые цепи представлены вне додекаэдра. |
||||||
|
|
|
|
Наш
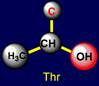
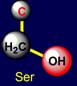
анализ будем проводить сверху вниз. В самом верху справа и слева распологаются боковые цепи серина
(Ser - справа) и треонина (Thr -
слева), обе имеют С-ОН-группу, но треонин имеет еще и метильную
группу. Чуть
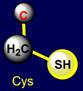
ближе к центру располагаются цистеин (Cys -
слева) и метионин (Met -
справа). Цистеин более легкая серусодержащая
боковая цепь, метионин – более тяжелая, у которой метильная
группа, связанная с атомом серы, препятствует проявлению слабокислых свойств,
характерных для цистеина. В
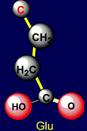
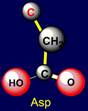
вершинах додекаэдра, связанных ребром с серином и треонином, ниже располагаются аспарагиновая (Asp - справа) и глютаминовая
(Glu -
слева) кислоты. Их боковые цепи содержат на конце группы О=С-ОН,
обладающие кислотными свойствами. Глютаминовая кислота на одну СН2-группу
длиннее аспарагиновой кислоты. Еще
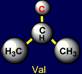
ниже, ближе к центру, располагается пара неполярных боковых цепей – валина (Val – справа) и изолейцина (Ile –
слева). Последний на одну метильную
группу длиннее валина. В
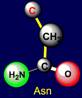
вершинах, связанных ребрами с цистеином и метионином, располагаются аспарагин
(Asn – справа) и глютамин (Gln –
слева). Это нейтральные боковые цепи, способные к образованию водородных
связей. Имеют одинаковую группу O=C-NH2,
но цепь глютамина длиннее на одну СН2-группу. Вершины, занимаемые аспарагиновой и глютаминовой кислотами,
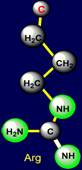
связаны с вершинами, в которых расположены боковые цепи аргинина (Arg –
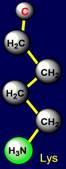
справа) и лизина (Lys – слева). Обе аминокислоты
проявляют щелочные свойства. У лизина
– более длинная боковая цепь . С
вершинами аргинина и лизина связаны ребрами
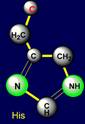
вершины, в которых располагаются боковые цепи гистидина (His –
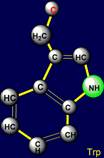
справа) и триптофана (Trp –
слева). Каждая из них содержит пятичленный цикл. У триптофана к нему присоединен
четырехзвенный фрагмент, образующий с пятичленным циклом дополнительный
шестичленный цикл. Обладают
слабощелочными свойствами. Ближе
к центру внизу располагается пара циклических боковых цепей, имеющих
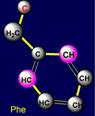
шестичленные циклы - фенилаланин (Phe –справа)
и тирозин (Tyr –
слева). При этом тирозин на атом кислорода длиннее, чем фенилаланин.
Обладают слабокислыми свойствами. |
|
|
|
|
Таким образом, мы
убедились, что распределение пар боковых цепей относительно плоскости I находится в точном соответствии с заданным принципом квази-зеркальной антисимметрии:
справа располагаются более легкие боковые цепи, слева - более тяжелые, а их
физические свойства в парах близки. |
||||||
Для дальнейшего
знакомства с антисимметриями аминокислот, которые
выявляются с помощью нашей модели, перейдите в разделы 4.2.2., 4.2.3 , 4.2.4.
или вернитесь в раздел
4.
Адрес для связи: amino-acids-20@yandex.ru